Валидация фармацевтического склада
Напишите нам, чтобы менеджер оперативно проконсультировал Вас и снял все вопросы по валидации фарм складов  .
.
Согласно принятым на международном уровне требованиям к хранению фармацевтической продукции (GMP, GDP, GSP), склады для хранения лекарственных средств обязаны проходить процедуру валидации. Это необходимо для того, чтобы фактически и документально подтвердить, что условия хранения на складе соответствуют требованиям к хранению на маркировках препаратов.
Вентиляционное оборудование и системы кондиционирования, установленные на складах, должны поддерживать атмосферу в помещении согласно установленным параметрам к тем препаратам, которые там хранятся. Эти условия должны сохраняться вне зависимости от времени года, погодных условий или времени суток.

Процесс проведения валидации на фармацевтическом складе
Процедура валидации складского помещения состоит из нескольких этапов.
Первый этап – квалификация проекта фармацевтического склада. Она начинается до того, как запускается строительство фармацевтического склада и заключается в том, чтобы проанализировать документы проекта. Это необязательный, но очень важный этап, поскольку позволяет выявить критические моменты в будущем строительстве и исправить их.
Второй этап – квалификация монтажа. Основные методы в данном случае – визуальный контроль и соотнесение с чертежами и спецификацией. На данном этапе необходимо проверить все проектные документы, инструкции по пользованию вентиляционными системами, системами отопления, автоматизации фармацевтического склада и т.д. На этом же уровне необходимо откалибровать оборудование для мониторинга показателей температуры и влажности.
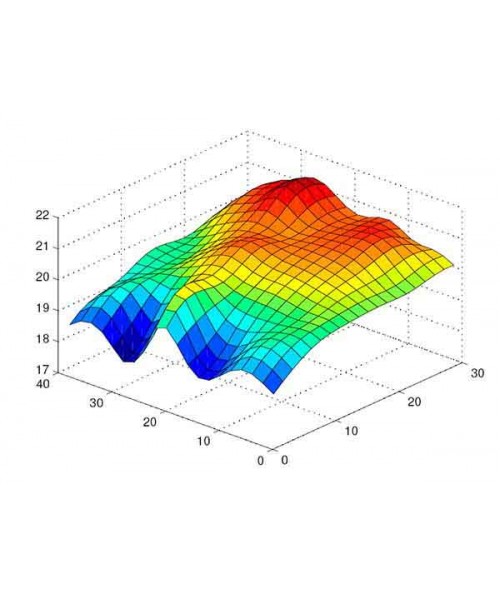
Третий этап – квалификация функционирования. Процедура проводится после того, как с успехом завершен предыдущий этап монтажа. На данном этапе проводится картирование склада при помощи специальных логгеров температуры и уровня влажности. Использовать в этом случае тепловизоры не рекомендуется, а инфракрасные термометры могут быть использованы только как дополнительное оборудование для определения рисков. Картирование представляет собой поиск максимально холодной и максимально горячей точек в помещении, а также точки, в которой определяется наибольшее колебание температурного показателя. По результатам этой процедуры вычисляются точки, где должны будут размещаться датчики для мониторинга.
После того, как завершен третий этап, необходимо оформить письменные методики, завершить ряд работ, не имеющих отношения к дистрибьюторской деятельности, закончить процесс обучения обслуживающего персонала. Только после этого возможно полноценное и безопасное с точки зрения хранения лекарственных препаратов функционирование фармацевтического склада.
Четвертый заключительный этап – квалификация эксплуатации. На данном этапе выполняется картирование по той же схеме, что и на предыдущем этапе, однако склад при этом заполнен лекарственными препаратами. Показания снимаются на протяжении 3 суток, при этом желательно, чтобы склад был максимально заполнен. В этом случае может быть смоделировано наихудшее развитие событий. Процесс картирования на этапе эксплуатации рекомендовано производить дважды в год – в холодное и теплое время года.
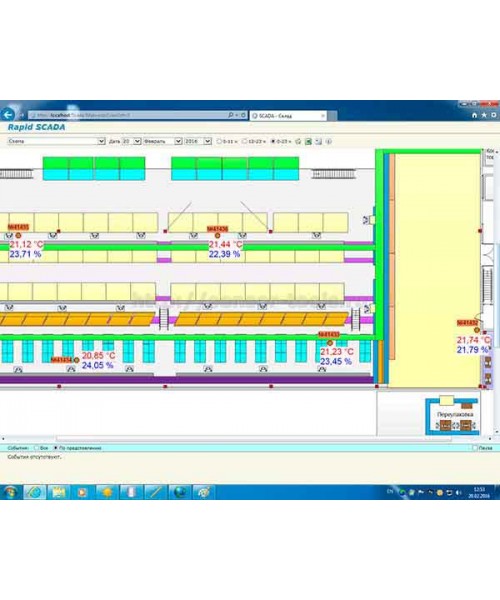
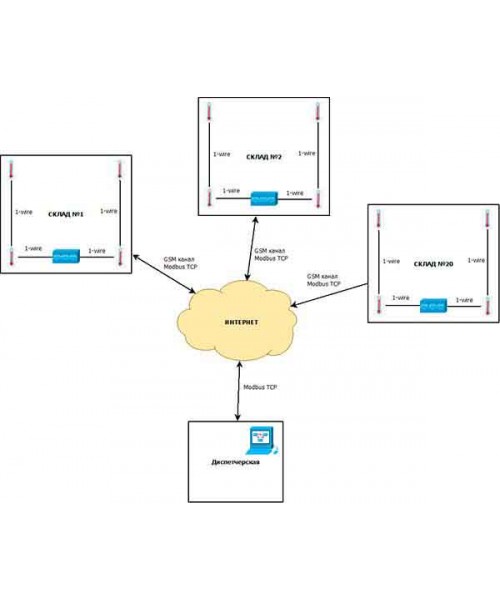
Валидация складского помещения для лекарственных препаратов должна проводиться периодически. Интервал между проведением процедуры зависит от показаний, которые предоставляют системы мониторинга. Такая система поставляет информацию о том, в каком техническом состоянии находится оборудование на складе, какие риски возможны в его работе, каков прогноз остаточного ресурса и т.д.
Напишите нам, чтобы менеджер оперативно проконсультировал Вас и снял все вопросы по валидации фарм складов  .
.